- Home
- 生化学(セルフリー)プロファイリング/スクリーニング アッセイ受託サービス
- ResidenceTimer™ キナーゼ蛋白質相互作用解析サービス
ResidenceTimer™
キナーゼ蛋白質
相互作用解析サービス
ResidenceTimer™ はカルナバイオサイエンス提供のビオチン化キナーゼタンパク質等を用い、SPR(Surface Plasmon Resonance、表面プラズモン共鳴)法による化合物とキナーゼ蛋白質の相互作用を速度論的に解析するサービスです。分子間相互作用検出用に開発された高感度SPR機器、Biacore T200 (Cytiva)を用いて経時的に観察したアフィニティーセンサーグラムから2分子間の結合特異性を確認、結合親和性をカイネティクス解析致します。
生物学的アッセイだけでは知りえない物理化学的な情報を得ることは化合物の真の特徴を知るうえでとても重要です。
市販されている薬剤の中には、標的分子との結合時間が長いために、血漿中からの消失半減期よりも長く標的分子に作用し、酵素アッセイで得られたIC50やKDから推測されるよりも強い効果を示す化合物があることが知られています。本サービスでの測定はn=2以上5濃度で行われ、化合物の結合速度定数(Ka)、解離速度定数(Kd)、解離定数(KD=Kd/Ka)、residence time (τ =1/Kd) をパラメーターとした測定結果をご報告致します。ATPバインディングポケット結合化合物のみならず、アロステリック効果をしめす非ATPバインディングポケット結合化合物にも対応します。
- <ご利用ガイド>
- サービスの流れ
- 被験物質の取り扱いについて
- ResidenceTimer™ サービス申込書
結合特性による薬剤候補の差別化
Residence Time(薬物滞留時間)の測定は、候補薬剤の競合化合物との差別化に役立ちます。ターゲットに数時間滞留する薬剤は、薬剤が全身から排出された後も薬力学的効果が持続するという利点があります。ResidenceTimer™プロファイリング サービスでは、他の薬剤と比較した候補薬剤の明確な薬理学的特徴づけとなるメカニズムに基づいた根拠を提供します。
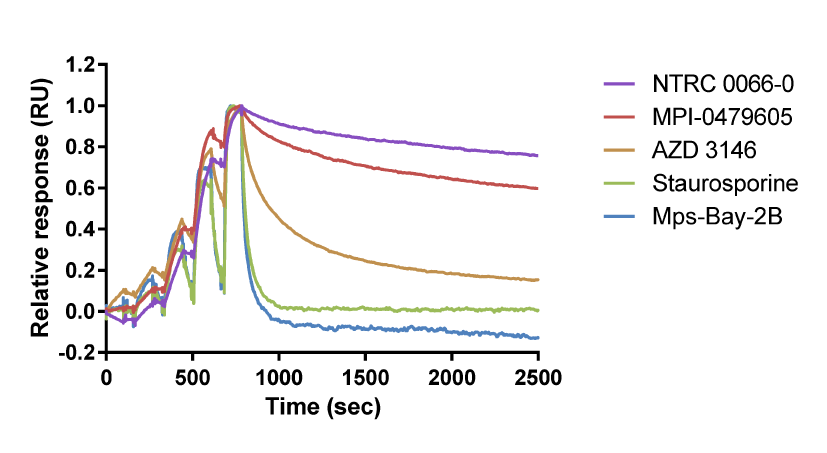
| Compound | ka(M-1 s-1) | kd(s-1) | KD(M) | t1/2(s) |
|---|---|---|---|---|
| NTRC 0066-0 | 5.10E+05 | 2.20E-04 | 4.30E-10 | 3185 |
| AZD 3146 | 3.50E+07 | 1.80E-01 | 5.00E-09 | 4 |
| MPI-0479605 | 1.60E+06 | 9.70E-04 | 5.90E-10 | 718 |
| Mps-Bay-2B | 2.20E+06 | 2.20E-02 | 1.00E-08 | 31 |
| Staurosporine | 6.70E+05 | 1.60E-02 | 2.50E-08 | 42 |
左: TTK 阻害剤の結合曲線の重ね合わせ。TTKに対する結合ではNTRC 0066-0 のResidence Timeが最も長く、StaurosporineとMps-Bay-2B は短い (Maia et al., 2015)。
上: TTK 阻害剤の TTK に対する結合パラメータ。
結合速度と解離速度による速度論的選択性
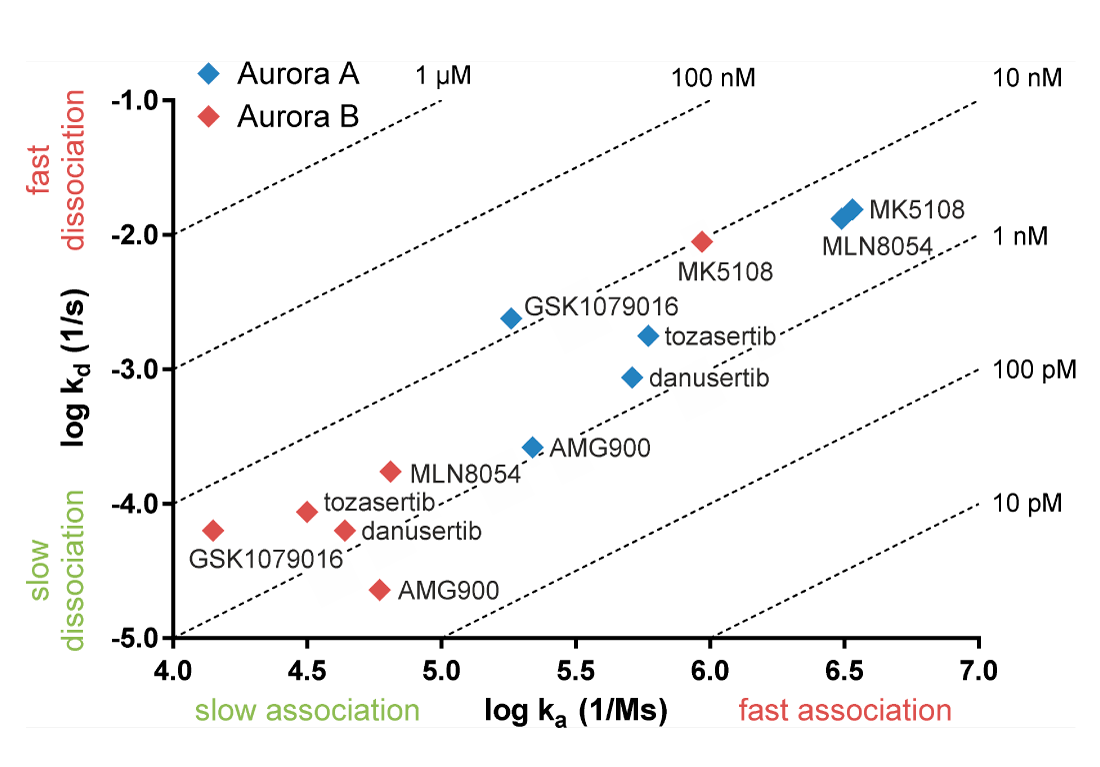
薬物の結合速度と解離速度は、同じ標的に対して同様の親和性を持つ化合物間で異なることがあります。下左図は、評価に用いられたすべての Aurora 阻害剤のAurora A と B に対する親和性が 1-10 nM と同様であるにも関わらず、結合速度と解離速度では明らかな差があることを示しています(Willemsen-Seegers et al., 2017)。Pan-Aurora阻害剤 danusertibは、表に示すとおりAurora A と B に対する親和性が同等ですが、解離率ではAurora Aとの比較でAurora B に対して 14 倍低くなっています。これは、danusertibのAurora B に対するResidence TimeがAurora A に対するものよりかなり長いことを意味します。特にResidence Time測定値が血中濃度半減期(消失半減期)を超える化合物の場合は、IC50 値または KD値に基づいて選択性を決定するよりも、速度論的選択性に基づく方が生体内効果の予測に役立ちます。
| danusertib | KD(M) | kd(s-1) |
|---|---|---|
| Aurora A | 1.69E-09 | 8.68E-04 |
| Aurora B | 1.44E-09 | 6.26E-05 |
左: Auroraキナーゼ阻害剤の結合速度(x軸)と解離速度(y軸)のグラフ。点線は、オン・オフ速度から計算された平衡親和定数(KD)を示します。
上: Danusertib の Aurora A および B に対する親和性と解離速度。速度定数は対数値の平均です。
Oncolines社提供のSPR測定の優位点
- センサーチップへの固相化が難しいターゲットも多数評価済み。各評価済みアッセイのサンプルセンサーグラムをターゲットリストでご確認頂けます(リストに無いターゲットについてはご相談下さい)
- ビオチン化蛋白質を用いての測定では、ビオチン分子一つだけがラベリングされたビオチン化キナーゼによるばらつきの無い固相化で非特異な相互作用を軽減(ターゲットリスト上のアッセイに使用されているリガンドは全て当社ビオチン化タンパク質製品です)
- ターゲットを中性PHで固相化することによりキナーゼタンパク質の活性低下軽減を実現
- 全ての試験が均一バッファーで行われる為ターゲット間の比較評価が容易
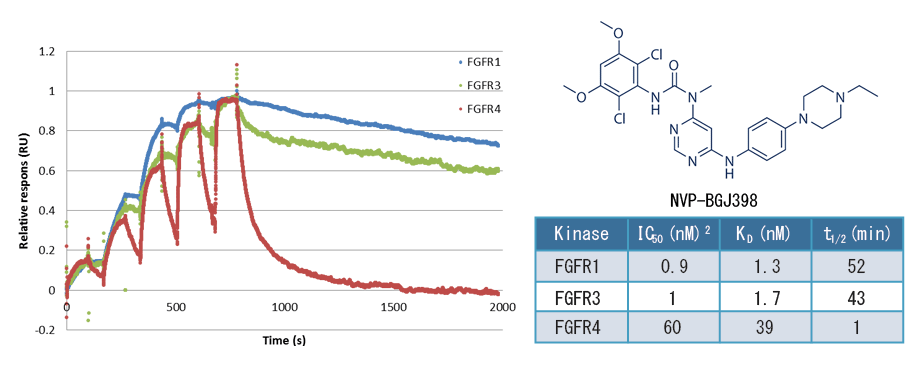
NVP-BGJ398に対するFGFR 1,3,4のシングルカイネティクスカーブ
異なるサブタイプに対する結合・解離の違いを知る事ができる
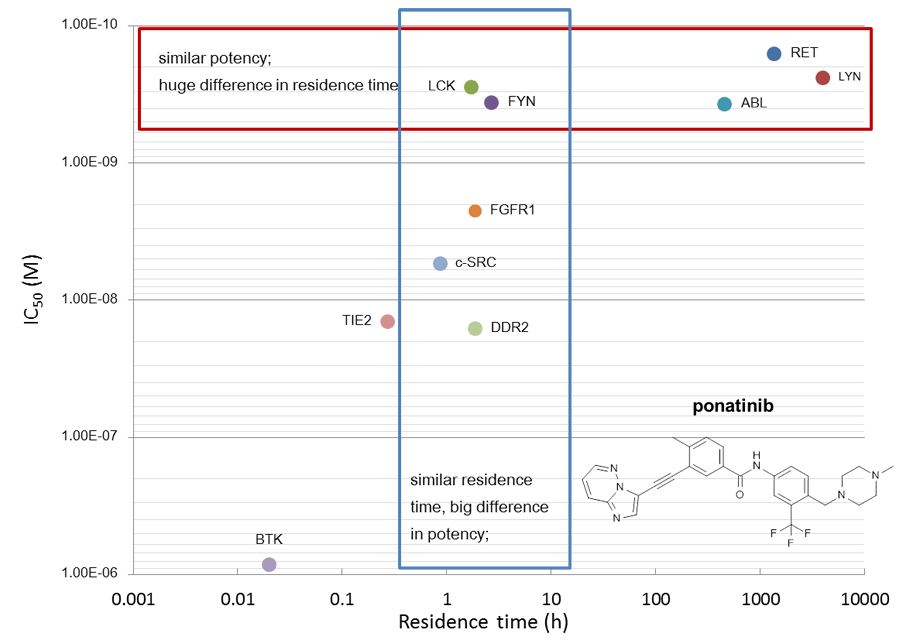
Ponatinibに対する酵素アッセイ結果とResidence Time測定結果の相関性
同程度のIC50値を示すターゲット間ではResidence Timeを測定することにより、化合物のターゲットに対する真の結合能を見極めることができる
- センサー表面に固相化されたキナーゼ蛋白質への結合だけを検出でき、バックグラウンドノイズが少ない高感度検出
- シングルサイクルカイネティクス解析法でリガンドとなるキナーゼタンパク質の活性低下軽減
- センサー表面で起こる屈折率の変化をリアルタイムに検出
- 屈折率の変化を検出するので、標識などを不要としたダイレクト検出
- センサー表面からのごく狭い範囲内のターゲット分子の変化だけを読み取る為、少量の化合物で測定OK
関連論文
Compound Selectivity and Target Residence Time of Kinase Inhibitors Studied with Surface Plasmon Resonance
http://dx.doi.org/10.1016/j.jmb.2016.12.019
Inhibition of the spindle assembly checkpoint kinase TTK enhances the efficacy of docetaxel in a triple-negative breast cancer model
- Oncolines B.V. (旧 Netherlands Translational Research Center B.V., NTRC) について
- Oncolines B.V.はオランダ・Oss市にある中核的研究施設内の拠点から、オンコロジーおよびがん免疫療法分野において開発薬剤/医薬品候補の差別化を追求する世界中の製薬・バイオテック企業へ精密医療サービスを提供する企業です。データ解析等で卓越した専門技術を備えたエキスパートで構成されており、薬剤の特徴、活性、選択性の見極め、他の薬剤との差別化を質の高い一連のサービスでサポート致します。同社は2011年の創設後2021年にNetherlands Translational Research Center B.V. (NTRC)からのスピンオフを経て2023年よりSymeres Netherlands B.V.のdaughter companyとなりました。
- https://www.oncolines.com/

