BTK阻害剤
docirbrutinib (AS-1763)
非共有結合・野生型/汎変異型BTK阻害剤
- 標的
- BTK (ブルトン型チロシンキナーゼ)
- 対象疾患
- 血液がん
- モダリティ
- 低分子化合物
- 開発ステージ
- フェーズ1b 用量拡大パート(米国)
- 臨床試験
- https://clinicaltrials.gov/study/NCT05602363
作用機序
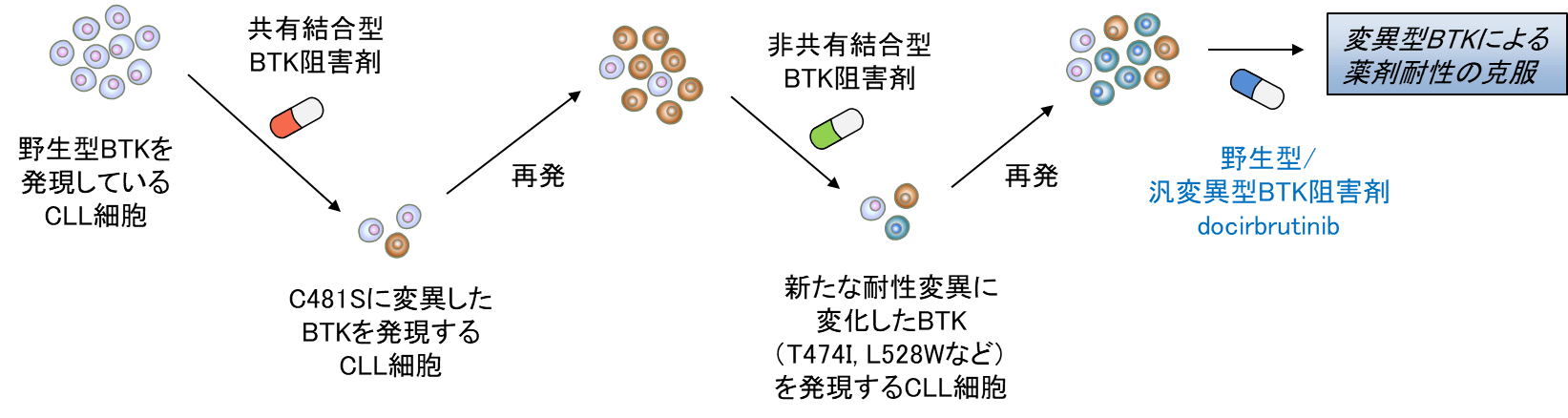
BTKは、B細胞の分化・増殖に関与するB細胞抗原受容体(BCR)シグナル伝達に重要な役割をしていることが知られており、血液がんの重要な治療標的として認識されています。共有結合型BTK阻害薬は慢性リンパ性白血病(CLL)を含む成熟B細胞腫瘍の有効な治療薬として幅広く使われていますが、これらBTK阻害剤に対する薬剤耐性が深刻な問題となってきています。近年、耐性患者においてC481Sが変異したBTKが高頻度に見い出され、この変異がBTK阻害剤の共有結合を妨げ阻害活性を低下させることが主な薬剤耐性の原因と考えられています。C481S 以外にも、非共有結合型BTK阻害剤に対する新たな耐性変異が報告されており、C481S耐性変異だけでなく、その他の変異型BTKにも有効な野生型/汎変異型BTK阻害剤の開発が非常に望まれています。
非臨床試験
docirbrutinibは、既存の共有結合型・非共有結合型BTK阻害剤に対する新たな薬剤耐性変異型BTK (C481S、T474x、T316x、L528x) を強く阻害します。また、docirbrutinibはびまん性大細胞型B細胞リンパ腫(DLBCL)マウスモデルで強い抗腫瘍効果を示したほか、 Bcl-2阻害薬との併用において優れた相乗効果も確認されています。
臨床試験
健康成人を対象としたdocirbrutinibの経口投与による単回投与用量漸増フェーズ1試験を実施した結果、最大用量である600 mgまでの安全性、忍容性及び良好な薬物動態プロファイルが確認され、薬力学作用の指標であるB細胞の活性化を100 mg以上で強く阻害しました。
上記結果を受け、2023年8月から米国において多施設共同試験として、患者を対象としたdocirbrutinibの非盲検フェーズ1b試験を開始しています。
当該フェーズ1b試験は2ライン以上の全身治療歴を有する慢性リンパ性白血病(CLL)・小リンパ球性リンパ腫(SLL)およびB細胞性非ホジキンリンパ腫(B-cell NHL)の患者を対象としており、用量漸増パートと用量拡大パートから構成されています。用量漸増パートでは、最大耐用量(MTD)および用量制限毒性(DLT)を決定することを主目的とし、副次的に安全性、忍容性、薬物動態、さらに有効性についても評価します。用量拡大パートでは、用量漸増パートで推奨された複数の用量で症例を追加し、安全性、有効性、薬物動態を調査し、フェーズ2試験の推奨用量(RP2D)を決定することを目的としています。
用量漸増パートでdocirbrutinibの高い安全性と忍容性、並びに治療効果の期待できる十分な血中薬物濃度と高い全奏効率を確認したことから、2024年9月に用量拡大パートを開始いたしました。本用量拡大パートは、CLL・SLL患者を対象としたコホート1、B-cell NHL患者を対象としたコホート2、およびピルトブルチニブ投与歴のある患者を対象としたコホート3の3つのコホートで構成されます。
フェーズ1b試験の初期結果として、docirbrutinibの安全性と良好な薬物動態プロファイル、並びに共有結合型BTK阻害剤やBCL2阻害剤などを含む2ライン以上の治療が行われたCLL患者およびマントル細胞リンパ腫(MCL)患者において高い全奏効率と持続的な臨床効果を示すことが確認されています。
参考文献
- Docirbrutinib (AS-1763), a novel non-COVALENT pan-mutant BTK inhibitor, demonstrates durable clinical responses in patients with previously treated B-cell malignancies: Data from an ongoing Phase 1b study, 67th American Society of Hematology Annual Meeting 2025
- Docirbrutinib (AS-1763), a novel non-COVALENT BTK inhibitor, demonstrates efficacy in BTK inhibitor-resistant mutant cells, 67th American Society of Hematology Annual Meeting 2025
- Preliminary Results from a Phase 1b Study of Non-covalent Pan-mutant BTK Inhibitor Docirbrutinib (AS-1763) in Patients with Previously Treated B-cell Malignancies, European Hematology Association 2025 Congress
- Preliminary Results from a Phase 1b Study of Non-Covalent Pan-Mutant BTK Inhibitor Docirbrutinib (AS-1763) in Patients with Previously Treated B-Cell Malignancies, 66th American Society of Hematology Annual Meeting 2024
- Impact of Docirbrutinib (AS-1763) Treatment in CLL: Preclinical Data and Early Clinical Biomarkers, 66th American Society of Hematology Annual Meeting 2024
- Preliminary safety and efficacy results from a Phase 1b study of oral non-covalent BTK inhibitor AS-1763 in patients with previously treated B-cell malignancies, European Hematology Association 2024 Hybrid Congress
- Trial in Progress: A Phase 1b Study of AS-1763, an Oral, Potent and Selective Noncovalent BTK Inhibitor, in Patients with Previously Treated Chronic Lymphocytic Leukemia/Small Lymphocytic Lymphoma or Non-Hodgkin Lymphoma, 65th American Society of Hematology Annual Meeting 2023
- Characterization and Preclinical Evaluation of AS-1763, an Oral, Potent and Selective Noncovalent BTK Inhibitor, in Chronic Lymphocytic Leukemia, 65th American Society of Hematology Annual Meeting 2023
- Safety, pharmacokinetics, and pharmacodynamics of AS-1763, a highly selective, orally bioavailable, non-covalent BTK inhibitor, in healthy volunteers, American Association for Cancer Research Annual Meeting 2022
- Discovery of AS-1763: A Potent, Selective, Noncovalent, and Orally Available Inhibitor of Bruton's Tyrosine Kinase. J Med Chem. 2021 Oct 14;64(19):14129-14141.

